1. 前言
1817年,瑞典化学家约恩斯·雅各布·贝采利乌斯(Jöns Jacob Berzelius)在研究硫酸的一种杂质时发现的新元素,并以希腊月亮女神的名字将该元素命名为Selene,即硒。
在硒被发现之后,人们很快认识到它的重要性,直至今天,研究人员依然在持续研究其性质与作用。与月亮有光明和黑暗两面相似,硒也有两面性:它对各种生物体既是有毒的,又是必不可少的。近年来,含硒化合物的设计和合成引起了人们的极大兴趣。各种有机硒化合物已被报道,而含Se的杂环化合物作为治疗一系列疾病(包括癌症、中风和糖尿病)的潜在药物,引起大量关注。
Wei Hou等近发表于J. Med. Chem. 的综述文章回顾了各种Se化合物及其相应生物活性的案例研究,介绍了Se在药物化学中应用的新进展。

2. 硒元素:理化性质影响生物活性
含硒的化合物,如硒醇、硒氧化合物、硒酯、硒酰胺和硒酸酐,通常比它们的含硫对应物表现出更强的生物活性。由于Se与S元素之间存在着的微妙的化学差异,使含Se化合物活性增加。例如,Se的尺寸比S大,导致外层价电子的结合更松散,同时,Se═O双键较大的杂化轨道和较长的键长导致较弱的π重叠,更容易被还原,这样,含硒化合物的抗氧化性、清除自由基能力更强(表1)。Se的化学特性影响了其药理活性,因此,了解这些关系对合理设计、开发含硒药物具有重要意义。
表1. Se和S的化学性质比较

(数据来源:J. Med. Chem.)
2.1. 抗氧化剂:硒作为双电子和单电子转移(SET)的还原剂来清除ROS
含硒分子著名的生理活动是其抗氧化性。重要的是一系列的硒蛋白,它们利用酶活性部位的Sec残基催化氧化还原反应,保护生物体免受氧化压力。此外,许多含硒的小分子通过清除ROS显示出良好的抗氧化活性。它们出色的还原能力归功于Se的强亲核能力和更松散的外价电子结合,使得Se化合物可以作为突出的双电子和单电子转移还原剂。
2.2. 促氧化剂:硒作为SET还原剂来诱导ROS
除了抗氧化作用外,含硒化合物也被发现具有促氧化的特性,并在高浓度下诱发ROS的产生。值得注意的是,为了支持快速的细胞分裂和增殖,癌细胞通常会进行反常的新陈代谢,并产生比正常细胞更多的ROS。因此,为了对抗更高水平的ROS,癌细胞会上调其抗氧化蛋白,如GPx、谷胱甘肽-S-转移酶(GST)和TrxR,迫使这些细胞大化其抗氧化能力,随后比正常细胞更容易产生额外的ROS。因此,Se物种有益的促氧化特性表明它们有可能被用作抗癌治疗药物。
2.3. 氧化剂:容易形成Se-S加合物
Se-X(X=Se、O、S和N)键的低能量σ*轨道使相应的Se化合物作为电子接受体相当活跃。同样,Se═O键表现出明显的双极性,从而使其具有有利的亲电特性。这种良好的亲电性和氧化性使这些Se化合物能够与硫醇反应,导致硫醇氧化和蛋白质中Cys残基的修饰,这往往伴随着Se-S加合物中间体的形成。重要的是,当这种共价修饰具有选择性时,它有助于提高药物与靶点的结合亲和力并延长停留时间。然而,当这种修饰是非选择性的,可能会出现副作用。此外,Se-S加合物的形成倾向可能会干扰金属与硫的配位,从而影响金属的释放和稳态。
2.4. 提高化合物的吸收率
增加吸收,特别是被癌细胞吸收,是Se化合物的另一个突出特点,尽管癌细胞对Se的选择性吸收的机制仍未被完全理解。Se的较大尺寸和较软的特性可能导致Se化合物的亲油性和渗透性增加。如图5所示,EBS(图5a)、硒化物(图5b)、苯并硒酸盐(图5c)、硒酰胺(图5d)和Se-氯丙嗪(图5e)的cLogP值都比其S对应物大。然而,在含Se的芳香族杂环1,3-硒唑的情况下,发现与S类似物相比,cLogP有异常的减少(图5f)。
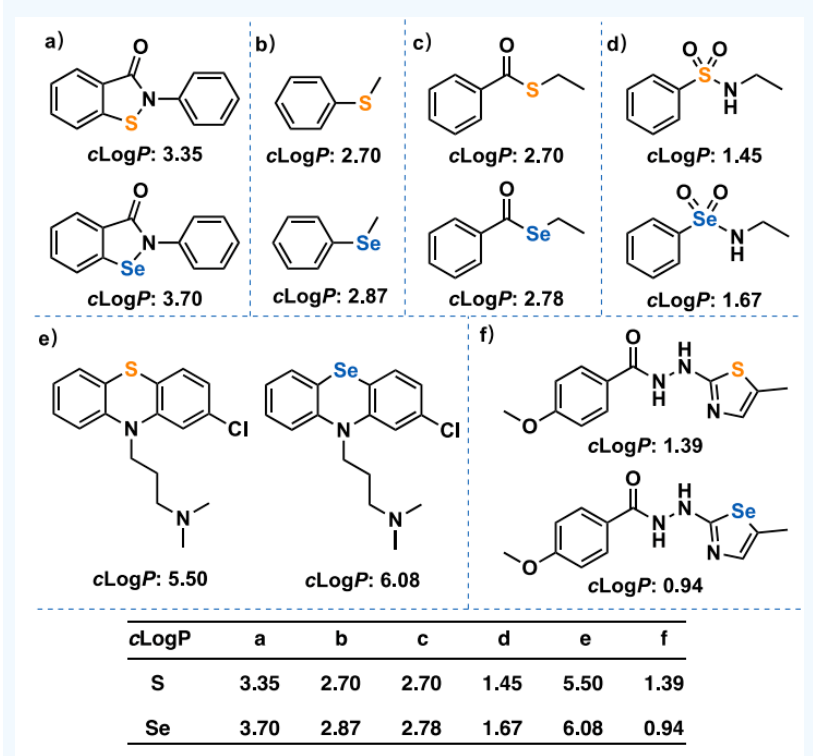
图5. Se化合物的cLogP值和其S对应物的比较
(图片来源:J. Med. Chem.)
2.5. Chalcogen Bonding
Chalcogen键(ChB)是缺电子的原子(S、Se和Te)的σ-空穴(低位σ*轨道)与电子供体原子(O和N)之间的相互作用。强的ChB相互作用至少和传统的H键一样强。其中,二价硫原子的ChB已被越来越多地应用于药物化学中的等价分子内氢键相互作用。与硫相比,Se更容易极化,因此,Se-ChB比S-CHB相互作用更强。Se-ChB相互作用已经逐渐被发现并应用于超分子化学和药物化学。
2.6. 硒的代谢
一般来说,一种药物的效力和疗效与它的代谢稳定性、途径和速率密切相关。含硒化合物的代谢稳定性和途径相互之间有很大的不同。此外,它们的生物活性往往是通过其代谢产物赋予的,从而使母体化合物成为前药。图7描述了基于动物研究的Se的代谢途径。
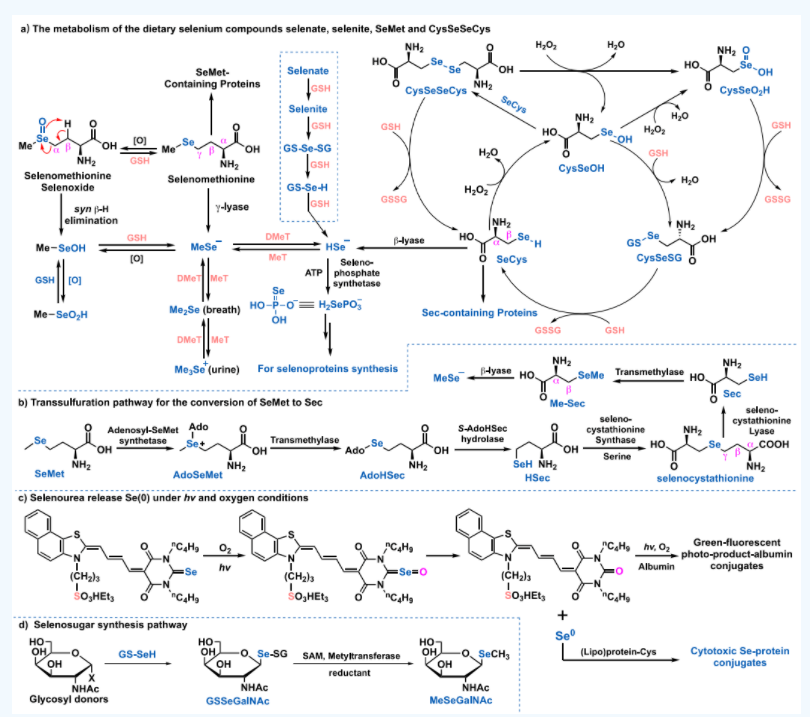
图7. Se化合物的代谢:(a) 膳食硒化合物硒酸盐、亚硒酸盐、SeMet和CysSeCys的代谢;(b) SeMet转化为Sec的转硫途径; (c)硒脲在有hv和氧气的条件下释放Se(0);(d)硒糖的合成途径
(图片来源:J. Med. Chem.)
3. 硒在药物化学中的运用
3.1. 含硒化合物
由于其强大的亲核能力,Se很容易与金属离子(Fe2+、Zn2+、Hg 2+等)形成复合物,发挥生理或药理作用(图8)。例如,硒酮8a2,麦角硫因8a1的Se类似物,已被确定为蓝鳍金枪鱼(Thunnus thynnus)血液中有机Se的主要化学形式。硒醇8a3是一种凝血酶可激活的纤维蛋白溶解抑制剂(TAFI),8a4是碳酸酐酶(CA)抑制剂。

图8.代表性的含Se衍生物:(a) 硒醇类;(b) 硒化物和二硒化物;(c) 硒氰酸酯、异硒氰酸酯、硒脲类、咪唑类、硒甲唑类和硒脲类苯磺酰胺类。
(图片来源:J. Med. Chem.)
3.2. 含硒的杂环化合物
含硒杂环代表了一大类Se化合物,它们被赋予了各种有前途的生物特性,如抗癌、抗炎和抗病毒活性。此外,硒杂环的环状结构(其中Se是sp2杂化的)防止它们释放元素Se,因此通常表现出更好的代谢稳定性。硒唑、硒二唑、噻硒唑和它们相关的融合类似物是重要的药效团。这些化合物中的一些已经成为优势结构,被用来产生各种有希望的药理作用(图9)。
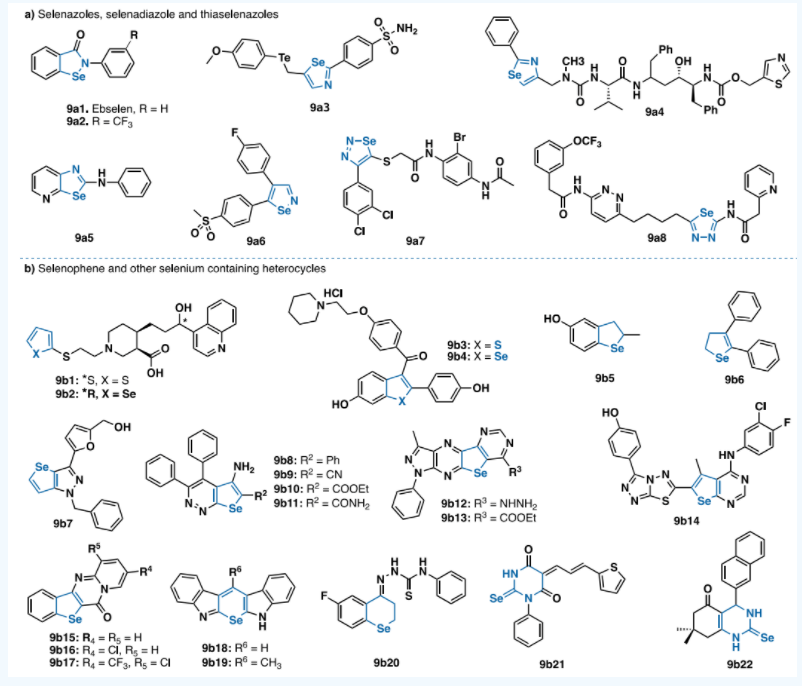
图9. 含硒的杂环:(a) 硒唑、硒二唑和硫硒唑;(b) 硒酚和其他含硒杂环
(图片来源:J. Med. Chem.)
3.3.硒修饰的天然产物
天然产物是经过进化优化的初级或次级代谢物,具有特殊的药理学特征,如结构复杂性、膜渗透性和生物功效,为药物发现提供了丰富的结构来源。目前,Se在天然产物修饰中具有大量运用,包括萜类、香豆素类、黄酮类、醌类、甾体类、维生素等(图10)。
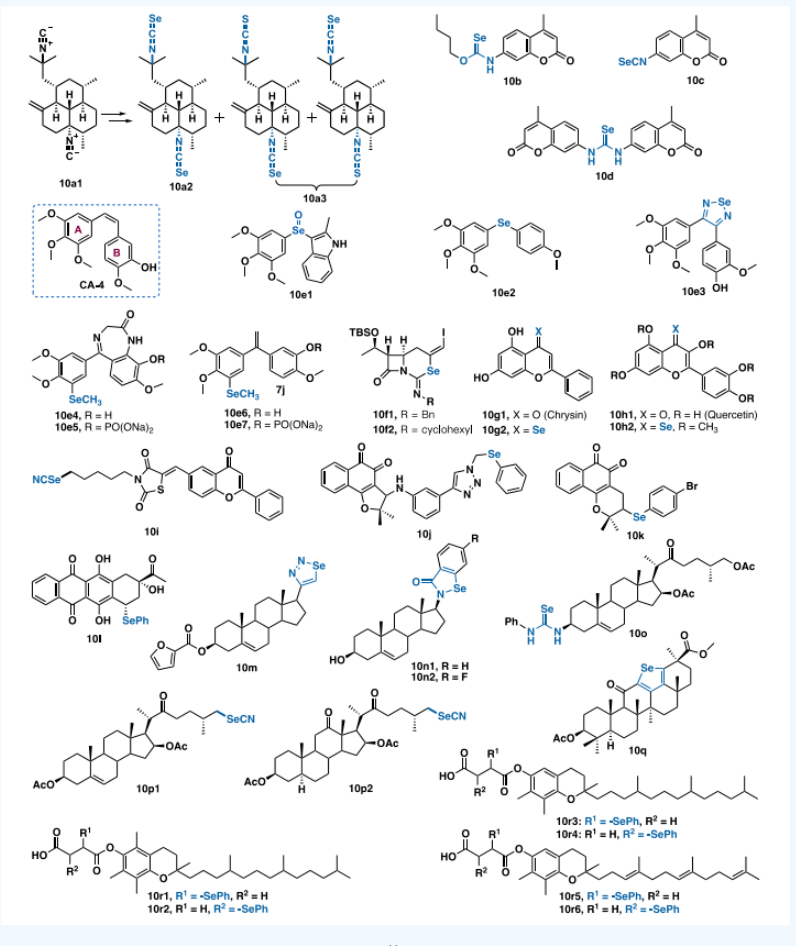
图10. 含硒萜类、香豆素类、黄酮类、醌类、类固醇和维生素
(图片来源:J. Med. Chem.)
Se在糖类衍生物中也有所应用,例如,将Se引入抗坏血酸衍生物,合成了一系列的6-O-l-抗坏血酸硒酯、用Se取代糖苷键中的氧原子等。(图11)。
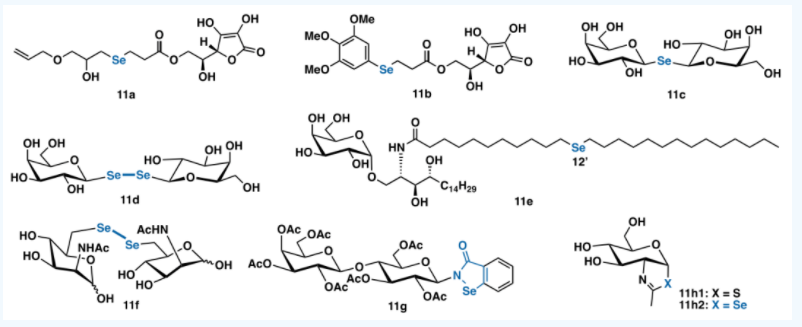
图11. 含硒的糖类衍生物
(图片来源:J. Med. Chem.)
将Se引入核苷类也是常见修饰策略,通过对糖基的氧或CH2进行生物替代,或者通过非天然杂环化合物均可将Se引入核苷中(图12)。
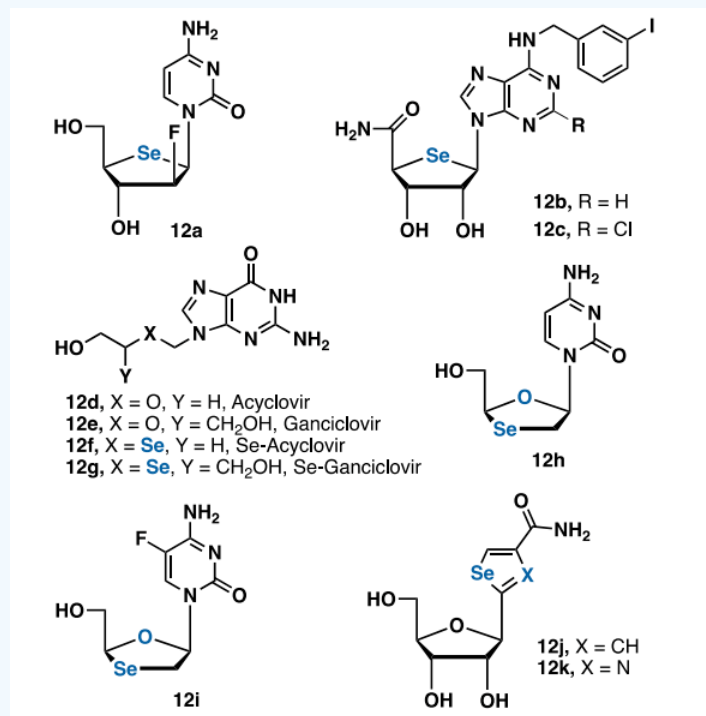
图12. 含Se的核苷衍生物
(图片来源:J. Med. Chem.)
4. 小结
从进化的角度来看,生物体利用硒蛋白来对抗氧化应激,深海鱼吸收了许多硒蛋白来对抗氧化应激和解毒重金属离子,包括汞。因此,合理利用Se无疑会对人类的生活和健康产生有益的影响。因此,Se已经逐渐成为杂环结构和天然产品改性方面的一个新兴的多功能角色。值得注意的是,由于Se的特殊属性,在引入药物分子前应全面考虑其对药理活性、理化性质、分子构象、代谢特性和潜在毒性的影响。为了推动有机硒化合物成为可行的临床治疗药物,仍然有问题需要解决,例如硒在人体的代谢途径、含硒化合物的确切作用靶点、含硒基团的稳定性等。

