前不久,诺华宣布其研发的靶向放射性配体疗法Pluvicto(lutetiumLu177vipivotidetetraxetan,177Lu-PSMA-617)获FDA批准上市,用于治疗PSMA阳性,且经过紫杉烷类化疗和雄激素受体信号通路抑制剂治疗的转移性去势抵抗性前列腺癌(mCRPC)患者。这也是首款FDA批准用于治疗这类mCRPC患者的靶向放射性配体靶向疗法。
“万物皆可偶联”!在偶联药物领域,除了目前我们大家所熟知的抗体偶联药物(ADC)之外,还有众多成员,其中便包括Pluvicto所在的偶联新赛道——放射性核素偶联药物(RDC)。
RDC是什么?
相信大家对于肿瘤放射性治疗(俗称:放疗)并不陌生,它对肿瘤具有强大的杀伤作用,但是不可忽视的安全性问题也限制了其临床的应用。
而放射性同位素(核素)药物的诞生为用好放疗这把“双刃剑”带来新的可能。在讨论核素药优势之前,我们先了解“放射性免疫治疗”的概念。放射性免疫治疗(RIT)是以单克隆抗体为载体,以放射性核素为弹头,通过抗体特异性结合抗原表达阳性的肿瘤细胞,将产生高能射线的放射性核素靶向到肿瘤细胞,并与肿瘤细胞特异性结合,实现对肿瘤的近距离内照射治疗,也称靶向放射性核素治疗。
有了单抗作为“引路人”,核素标记的药物在肿瘤病变部位浓聚,到达肿瘤这一特殊战场后,两者合作“火力交叉”共同对抗肿瘤细胞,从而达到治疗的目的。
核素偶联药物(RDC)属于核素药物的一种,主要由靶向配体(Ligand)、连接臂(Linker)、螯合物(Chelator)和核素(Radioisotope)构成。
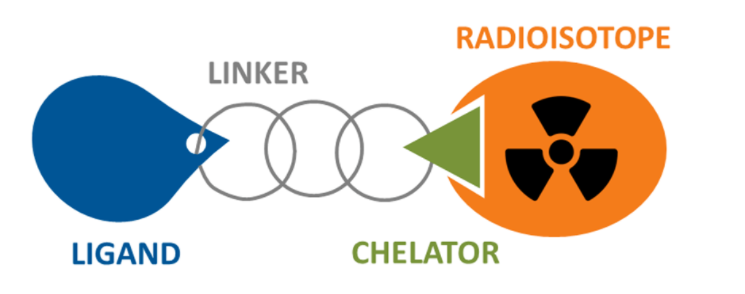
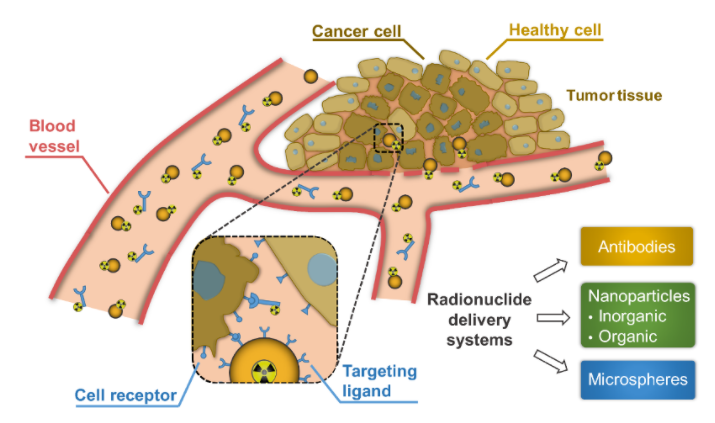
与ADC药物相似,利用抗体或小分子介导特异性靶向作用,将细胞毒性分子或成像分子如放射性核素递送至靶位置,从而将放射性同位素产生的放射线集中作用于组织局部,在高效精准治疗的同时降低全身暴露对其他组织造成的损伤。核素带来的放射性射线所产生的能量可破坏细胞的染色体,使细胞停止生长,从而消灭快速分裂和生长的癌细胞。
与ADC药物不同,RDC载荷是放射性核素,既可用于诊断也能实现治疗功能。在组成上,RDC也略有差异,需要添加螯合毒素的特定官能团结构(Chelator)。当前常用的配体包括小分子(如PSMA-617)、抗体等,放射性同位素包括作为示踪剂的68Ga、64Cu,以及用于治疗的177Lu,213Bi等。
打破魔咒,难靶点PSMA开发成功
RDC虽然不似ADC药物那样火热,但已经有不少新药开发成功案例。其中,LUTATHERA是FDA批准的第一个治疗胃肠胰神经内分泌肿瘤的放射性药物,2019年销售额4.41亿美元,同比增长167%。该产品已经于2020年7月在国内提交临床申请。
另一款获FDA批准的RDC药物是加州大学开发的GALLIUMGA68PSMA-11,这是第一个用于前列腺特异性膜抗原(PSMA)阳性病灶PET成像的药物,适用于疑似前列腺癌转移的患者,以及血清PSA升高疑似前列腺癌复发的患者。
从靶点上看,目前在研的RDC药物以靶向PSMA的项目居多。PSMA是前列腺癌中的重要分子靶标,在近20年来得到了广泛的研究。在诊断层面上,PSMAPET-CT已经展现了自己的优越之处,能够更准确的检测出转移灶,从而改变患者的治疗方案。
但过去一段时间里,基于PSMA靶点的药物发展并不顺利。例如,APVO414由于免疫原性而被终止研发、AMG160疗效有限、P-PSMA-101因为安全性问题曾一度被叫停……直到Pluvicto的出现第一次打破了PSMA的失败魔咒。
Pluvicto此次获批是基于其临床3期试验VISION的积极结果:在二线PSMA阳性的mCRPC(转移性去势抵抗性前列腺癌)患者中,617+佳标准治疗(SOC)对比SOC,中位OS达到了15.3个月vs11.3个月,将患者的死亡风险降低了38%;rPFS(放射影像学无进展生存期)更是达到了8.7个月vs3.4个月;并且617+SOC组的PR/CR达到了29.8%,SOC组仅有1.7%的PR。
目前在mCRPC的治疗中,临床表现好的方案是PARP抑制剂奥拉帕利。2020年5月奥拉帕利获批二线mCRPC适应症时,使用的PROfound研究数据显示,奥拉帕利单药,对比恩杂鲁胺,或阿比特龙+泼尼松,在A组BRCA1/2或ATM突变患者中,实现了19.1个月vs14.7个月的OS和7.4个月vs3.6个月的mPFS。
对比以上数据可以看出,Pluvicto目前披露的疗效数据在mPFS上比奥拉帕利略胜一筹,OS不相上下;安全性数据基本没差别,甚至不良反应发生率略低。
群雄逐鹿,RDC或成未来黄金赛道
随着在研产品的陆续获批上市,RDC药物市场近年来迎来了新的增量。据不完全统计,目前已有多款在研产品已经处于关键临床阶段。
例如:海外POINTBiopharma公司研发的另一款用于mCRPC的靶向放射配体疗法PNT2002(177Lu-PSMA-I&T)当前处于3期临床试验阶段,该疗法采用的PSMA配体与Pluvicto不同。此前的临床试验表明该药物对正常组织的辐射剂量处于安全范围内,对红髓的辐射低有望用于联合治疗。
拜耳研发的227Th-PelgifatamabCorixetan靶向PSMA,用于治疗mCRPC,当前正处于1期临床研究阶段。与诺华和POINTBiopharma采用177Lu产生β粒子不同,拜耳采用的227Th产生α粒子能够在更短的作用距离中对肿瘤产生更强的杀伤作用。此外,拜耳于2021年6月收购了NoriaTherapeutics和PSMATherapeutics,获得其研发的靶向PSMA的225Ac放射性疗法,处于临床前研究阶段。
远大医药是国内RDC龙头公司,较早开始布局RDC产品管线。在产品管线上,远大医药引进了Telix研发的多款RDC药物,包括用于诊断的TLX591-CDx、TLX250-CDx、TLX599-CDx和用于治疗的TLX591、TLX250、TLX101在大中华区(包括香港、澳门、台湾)的独家商业化权益。
其中用于诊断前列腺癌的TLX591-CDx已在美国和澳洲获批上市,并在巴西获得特别授权,准许正式获批前销售;用于诊断透明细胞肾细胞癌的TLX250-CDx已获FDA批准突破性疗法并于澳洲完成1期临床研究首例患者给药;用于治疗胶质母细胞瘤的TLX101已获FDA孤儿药资质认定;用于治疗前列腺癌的TLX591已于澳洲获批开展3期临床研究。另外,多款RDC药物在中国的注册工作也在积极的推进中,其中TLX591-CDx预计将于2022年第一季度向NMPA递交临床研究申请(IND)。
在2021年12月27日,远大医药还与德国ITMIsotopeTechnologiesMunichSE公司达成了产品战略合作,支付不超过5.2亿欧元的授权签约费及里程碑款项以获得ITM公司开发的用于诊断胃肠胰腺神经内分泌瘤的TOCscan®(68Ga-Edotreotide),用于治疗胃肠胰腺神经内分泌瘤的ITM-11(n.c.a.177Lu-Edotreotide)以及用于治疗恶性肿瘤骨转移的ITM-41(n.c.a.177Lu-Zoledronate)在内的3款RDC产品在大中华区(中国大陆、香港、澳门、台湾)的独家开发、生产及商业化权益,进一步扩充了公司的RDC产品管线。
结语
全球获批的放射性核素偶联药物极少,而且处于临床研究的项目也较为稀缺。随着国际制药巨头的加入和各大资本逐渐布局,RDC药物有望成为高速发展的新兴赛道。

