注:本文不构成任何投资意见和建议,以官方/公司公告为准。

5月19日,国家药监局药品审评中心(CDE)官网显示,广州百暨基因科技有限公司(以下简称“广州百暨”)申报的“自体抗CLL-1嵌合抗原受体T细胞注射液”临床试验申请获得受理。早在2022年12月30日,广州百暨“自体抗CLL-1嵌合抗原受体T细胞注射液”临床试验申请(受理号:CXSL2200512)获批,适应症为复发难治性急性髓系白血病(r/r AML)。

欧盟EMA孤儿药认定
2022年10月,获得欧洲药物管理局(EMA)孤儿药认定(ODD),用于治疗AML。

关于抗CLL-1 CAR-T产品
自体抗CLL-1嵌合抗原受体T细胞注射液是由广州百暨自主研发并拥有核心专利技术靶向CLL1的细胞疗法产品,具有抗体具有高特异性、高亲和力,持久、高效的癌细胞杀伤能力等优势。2021年6月,广州百暨在2021年美国临床肿瘤学会(ASCO)年会中口头报告数据显示,对11例患者输注CAR-T细胞后,CAR-T细胞可以在患儿体内快速、高效地扩增;总缓解率(ORR)高达81.8%(9/11),总疾病控制率(DCR)高达90.9%(10/11),10/11的患者在一个月内即对Anti-CLL1 CAR-T疗法产生积极响应。

广州百暨基因科技有限公司是广州七喜集团控股子公司,目前在广州市科学城已建立3000平米的研发和生产车间,并建立了一系列技术平台,包括新靶点抗体筛选平台,通用型的γδT/NK培养工艺,针对实体瘤的趋化因子平台等,多项产品推进临床阶段,希望能造福更多的肿瘤患者。
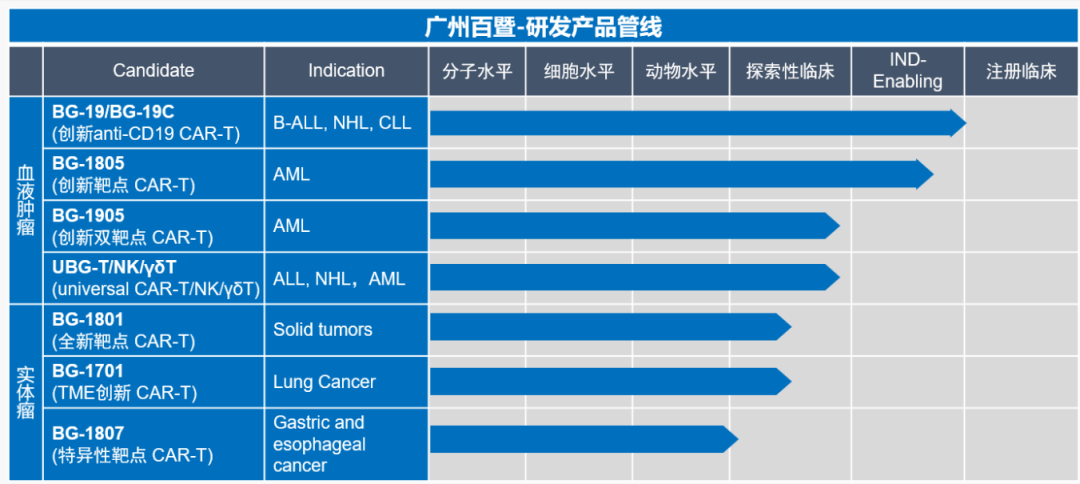
参考资料:广州百暨官微
版权声明:本文转自细胞基因治疗前沿,如不希望被转载的媒体或个人可与我们联系,我们将立即删除。

